 |
|
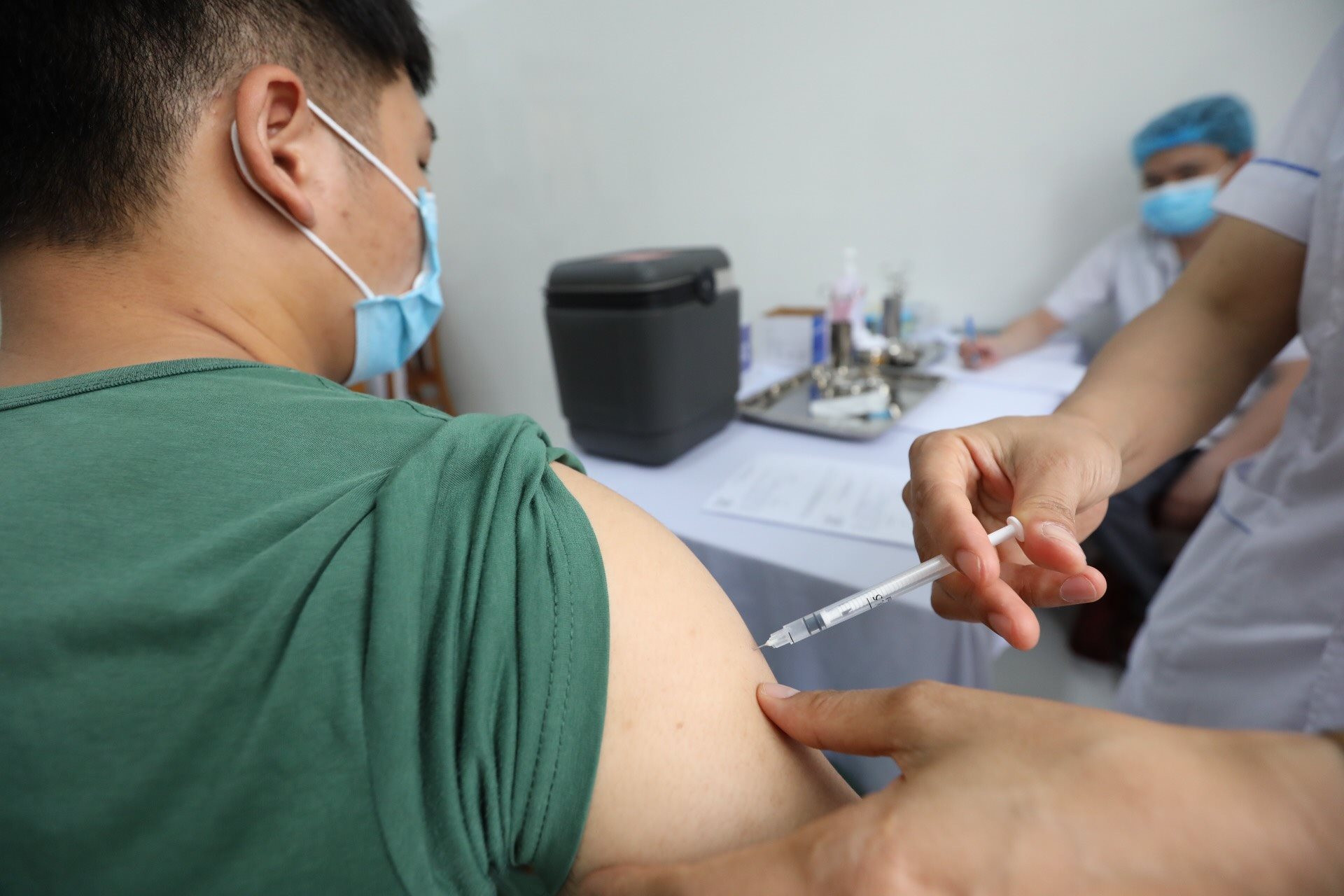
Tiêm vắc xin phòng COVID-19 Nano Covax cho người tình nguyện giai đoạn 3 |
Thực hiện chỉ đạo của Đảng, Chính phủ, ngay từ khi dịch bệnh COVID-19 xuất hiện ở Việt Nam, cùng với việc nỗ lực tìm kiếm, tiếp cận, đàm phán, trao đổi với các nhà sản xuất, đối tác phát triển, sản xuất, cung ứng vắc xin phòng COVID-19 trên thế giới, Bộ Y tế đã chỉ đạo các đơn vị nghiên cứu phát triển và sản xuất vắc xin trong nước chủ động, tích cực, khẩn trương triển khai các nghiên cứu phát triển, thử nghiệm lâm sàng vắc xin “made in Việt Nam”.
Việt Nam đang nghiên cứu, phát triển hai loại vắc xin phòng COVID-19
Đến nay, cả nước có 2 nhà sản xuất đang nghiên cứu, phát triển vắc xin phòng COVID-19, trong đó, có 1 loại vắc xin đã được phê duyệt thử nghiệm lâm sàng giai đoạn 3 là vắc xin Nanocovax của Công ty Cổ phần Công nghệ sinh học Dược Nanogen.
Do điều kiện cấp thiết về vắc xin phòng chống dịch bệnh, để thúc đẩy tiến độ nghiên cứu nhằm sớm có vắc xin phục vụ công tác phòng chống dịch, Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia đã tổ chức các cuộc họp, thảo luận kỹ và thống nhất cho phép triển khai gối đầu thử nghiệm lâm sàng giai đoạn 3, tuy nhiên vẫn phải đảm bảo đúng các quy định chặt chẽ về tính khoa học, đảm bảo chất lượng vắc xin.
Theo đó, ngày 11/6, Bộ Y tế đã có Quyết định số 2899/QĐ-BYT về việc phê duyệt đề cương nghiên cứu thử nghiệm lâm sàng giai đoạn 3 vắc xin Nanocovax phòng COVID-19.
Tổ chức nhận thử nghiệm lâm sàng là Học viện Quân Y và Viện Pasteur thành phố Hồ Chí Minh; địa điểm triển khai tại Học viện Quân Y, tỉnh Hưng Yên, Viện Pasteur thành phố Hồ Chí Minh, tỉnh Long An, tỉnh Tiền Giang và một số đơn vị đủ điều kiện theo quy định tại các tỉnh triển khai nghiên cứu. Đối tượng nghiên cứu từ 18 tuổi trở lên đáp ứng đầy đủ các tiêu chuẩn lựa chọn và không có bất kỳ tiêu chuẩn loại trừ nào theo đề cương nghiên cứu.
Số lượng đối tượng tham gia nghiên cứu thử nghiệm lâm sàng giai đoạn 3 dự kiến khoảng 13.000 người để đánh giá tính an toàn, đáp ứng miễn dịch và hiệu lực bảo vệ của vắc xin (bao gồm 1.000 đối tượng để đánh giá giữa kỳ về tính an toàn và sinh miễn dịch).
Ngoài ra, 1 loại vắc xin phòng COVID- 19 khác đang được thử nghiệm lâm sàng giai đoạn 1 là vắc xin COVIVAC của Viện Vắc xin và sinh phẩm y tế Nha Trang (IVAC). Hiện vắc xin này đang trong giai đoạn báo cáo giữa kỳ giai đoạn 1 để chuyển tiếp nghiên cứu giai đoạn 2 tại Thái Bình.
Vắc xin sẽ được sản xuất trên nền cơ sở vật chất hiện có. Cụ thể, IVAC dự kiến quy mô sản xuất khoảng 6 triệu liều vắc xin/năm và có thể nâng công suất khi được đầu tư; Nanogen dự kiến quy mô sản xuất khoảng 20 -30 triệu liều vắc xin/năm và có thể nâng công suất khi được đầu tư. Tuy nhiên, để nâng công suất các nhà sản xuất cần đầu tư thêm các trang thiết bị chuyên dụng và mở rộng nhà xưởng.
Thúc đẩy trao đổi, chuyển giao công nghệ sản xuất vắc xin từ nước ngoài
Bên cạnh việc nghiên cứu sản xuất vắc xin trong nước, Bộ Y tế cũng chỉ đạo mở rộng tìm kiếm hợp tác chuyển giao công nghệ sản xuất vắc xin từ nước ngoài để nhanh chóng có vắc xin phòng chống dịch bệnh cho Việt Nam.
 |
|
Bộ Y tế làm việc với Đại sứ quán Pháp về hợp tác trong công tác phòng chống dịch COVID-19, đặc biệt là việc tạo điều kiện để Việt Nam tiếp cận các nguồn vắc xin phòng COVID-19 |
Theo đó, ngày 7/5/2021, Bộ trưởng Bộ Y tế đã ban hành Quyết định số 2301/QĐ-BYT thành lập Ban Chỉ đạo Chương trình nghiên cứu chuyển giao công nghệ và sản xuất vắc xin phòng COVID-19.
Một doanh nghiệp Việt Nam đã thảo luận, đàm phán với Nhà sản xuất Hoa Kỳ về điều kiện chuyển giao công nghệ sản xuất vắc xin COVID-19 từ tinh chất mRNA (Vắc xin này chỉ cần tiêm 1 liều duy nhất 5 mg, có khả năng bảo vệ cao (dựa trên kết quả TNLS giai đoạn 1, 2), có nhiệt độ bảo quản 20C - 80C, hiện tại vắc xin đã kết thúc thử nghiệm giai đoạn 1, 2). Nhà máy đầu tư theo chuẩn công nghệ của nhà sản xuất sẽ có công suất 100-200 triệu liều/ năm dự định bắt đầu sản xuất từ Quý 4/2021 hoặc Quý 1/2022.
Công ty cổ phần tiến bộ quốc tế (AIC) đã hỗ trợ liên hệ với Công ty sản xuất vắc xin của Nhật Bản theo công nghệ tiên tiến.
Hiện nay, Công ty TNHH MTV Vắc xin và Sinh phẩm số 1 (VABIOTECH) đang xúc tiến đàm phán với đối tác Nhật Bản để sớm tiếp nhận chuyển giao công nghệ sản xuất vắc xin cho Việt Nam.
VABIOTECH cũng đã ký thỏa thuận với Quỹ đầu tư trực tiếp của Liên bang Nga về việc đóng ống vắc xin phòng COVID-19 Sputnik-V từ bán thành phẩm với quy mô 5 triệu liều/tháng bắt đầu từ tháng 7/2021, tiến tới chuyển giao công nghệ sản xuất với quy mô 100 triệu liều/năm.
Bên cạnh đó, tại cuộc làm việc với Đại sứ Pháp Nicolas Warnery ngày 8/6, Bộ trưởng Nguyễn Thanh Long bày tỏ mong muốn ngoài hỗ trợ qua cơ chế COVAX, phía Pháp cũng có những hỗ trợ khác về vắc xin cho Việt Nam. Hiện Sanofi và một số công ty dược khác của Pháp đang nghiên cứu, thử nghiệm vắc xin COVID-19 giai đoạn 3, Bộ trưởng mong muốn hai bên hợp tác trao đổi, chuyển giao công nghệ để giúp Việt Nam trong phát triển, sản xuất vắc xin.
Đại sứ Nicolas Warnery khẳng định mối quan hệ hợp tác y tế giữa Pháp và Việt Nam rất lâu đời với những chương trình hợp tác, hỗ trợ song phương, đa phương. Ông ghi nhận những đề xuất về tăng cường trao đổi để tiến tới chuyển giao công nghệ của Việt Nam. Các đề nghị của Việt Nam đang được phía Pháp nghiên cứu.
 |
|
|


.jpg)







.jpg)













